
Archivo de la categoría: Noticias


Investigación publicada en Proceedings of the National Academy of Science, evaluó efectos del aumento y disminución del hielo durante períodos glaciales e interglaciales, en once especies de estas aves marinas. Trabajo, liderado por científicos de Nueva Zelanda, contó con la participación de María José Frugone, investigadora chilena del Instituto de Ecología y Biodiversidad, IEB.

Análisis liderado por Alejandra Álvarez determina que, al inhibir una enzima específica en modelos de epilepsia, el avance de la patología se hace más lento. Resultados están orientados a desarrollar un tratamiento capaz de detener el avance de esta enfermedad neurológica. La futura terapia puede atravesar la barrera protectora del cerebro, aumentando su efectividad.

Enrique Mejías encabeza un proyecto PAI en la Comisión Chilena de Energía Nuclear que tiene como objetivo combatir esta enfermedad que daña a las larvas y crías de abejas. Para realizar el estudio el académico viajó a Valdivia, Futrono y Panguipulli, donde se reunió con asociaciones de apicultores de aquellas zonas para la recolección de muestras. La investigación también incluirá sitios de estudio ubicados en las regiones de Coquimbo, Valparaíso, Metropolitana y Los Lagos.
Un nuevo artículo de Scientific Reports le da un giro evolutivo a una pregunta clásica. En lugar de preguntar por qué tenemos cáncer, Leonardo Oña, de la Universidad de Osnabrück, y Michael Lachmann, del Instituto Santa Fe, utilizan la teoría de la señalización para explorar cómo han evolucionado nuestros cuerpos para evitar que tengamos más cáncer.

Las abejas melíferas del mundo enfrentan una crisis sin precedentes. Desde la década de 1940, el número de colmenas de abejas en los Estados Unidos se ha reducido de 6 millones a 2.5 millones. Una combinación de ácaros que matan colonias, patógenos virales y posiblemente pesticidas es en gran parte culpable. Ahora, los investigadores están aprovechando un aliado inusual en la lucha para traer de vuelta a las abejas: una bacteria que vive únicamente en sus entrañas. Al modificar genéticamente la bacteria para engañar al ácaro o un virus para destruir parte de su propio ADN, los científicos mejoraron la supervivencia de las abejas en el laboratorio y mataron a muchos de los ácaros que estaban parasitando a los insectos.
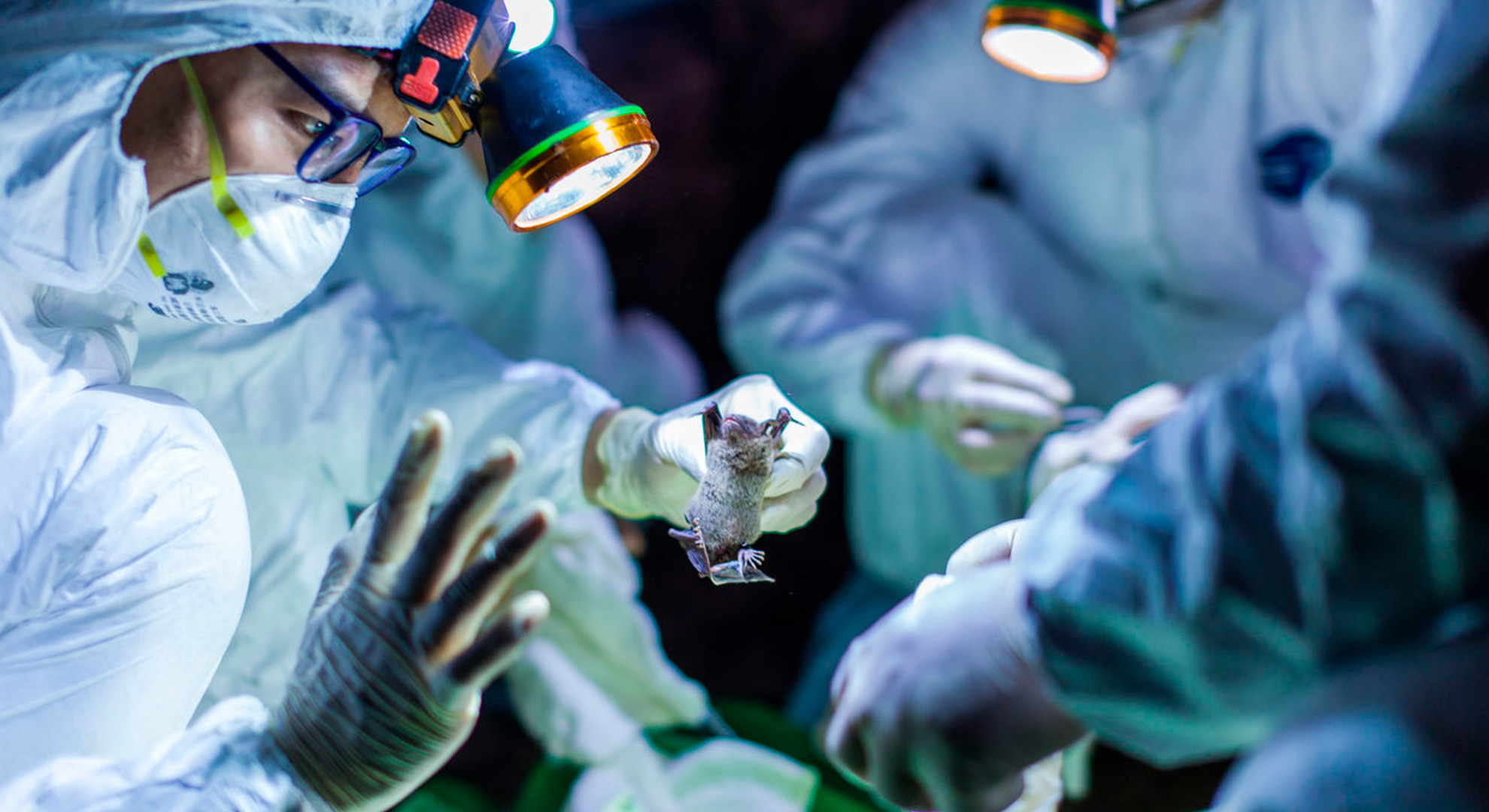
Esa cadena de galimatías aparentes es todo menos eso: Un fragmento de una secuencia de ADN del patógeno viral, denominado nuevo coronavirus 2019 (2019-nCoV), que está abrumando a China y asustando al mundo entero. Los científicos comparten públicamente un número cada vez mayor de secuencias completas del virus de los pacientes: 53 en el último recuento en la base de datos Global Initiative on Sharing All Influenza Data. Estos genomas virales se están estudiando intensamente para tratar de comprender el origen de 2019-nCoV y cómo encaja en el árbol genealógico de los virus relacionados que se encuentran en los murciélagos y otras especies. También han dado una idea de cómo se ve físicamente este virus recién descubierto, cómo está cambiando y cómo se puede detener.
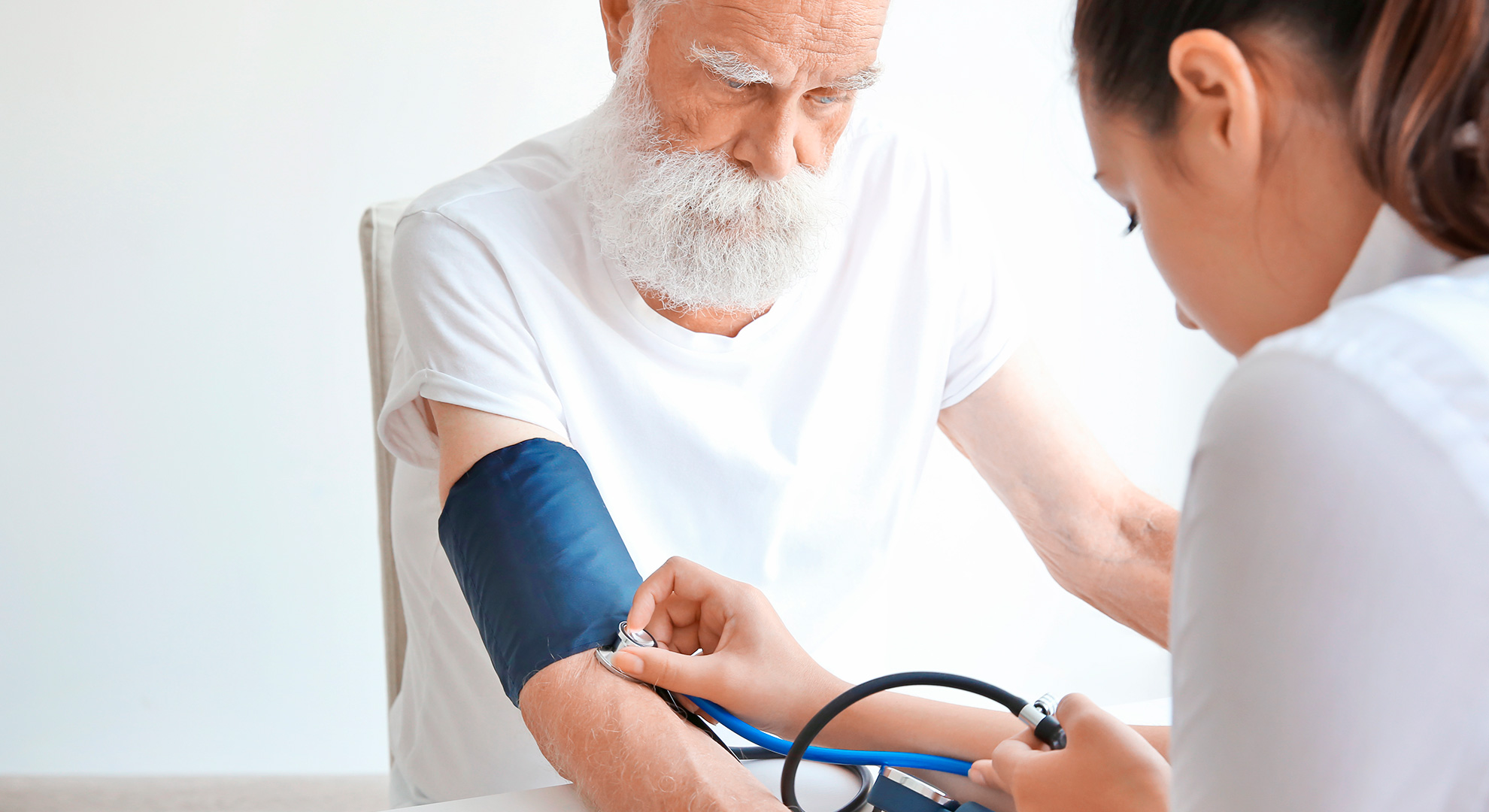
Reducir la presión arterial sistólica de una persona mayor a 120 mmHg o menos reduce el riesgo de enfermedad cardíaca, pero aumenta la posibilidad de cambios en los riñones.

Las bacterias patógenas, que causan enfermedades, son capaces de transmitir sus genes a sus similares no patógenas e inclusive a otros microorganismos. El problema es que este proceso también conlleva a que aquellas que se vuelven resistentes a los antibióticos, compartan su ADN a sus otras pares.
El dilema de la resistencia de los antimicrobianos ha avanzado de tal manera que la Organización Mundial de la Salud (OMS) la denominó como “una de las mayores amenazas para la salud mundial”. Creó hace unos años una entidad especializada en la supervisión de estos microorganismos y pronosticó que para el 2050 las muertes por cepas virulentas resistentes a los antibióticos pueden llegar a 10 millones anuales en todo el mundo.
A pesar del pésimo panorama, el equipo científico del IMII, liderado por Bueno, descubrió un proceso fundamental que llevan a cabo bacterias patógenas, como las que causan la salmonelosis y el cólera, para generar una infección sistémica en un organismo vivo, y con ello, abren la puerta para avanzar en la elaboración de fármacos y terapias más eficaces.
“Nosotros estamos pensando que la detección de estos mecanismos permitiría desarrollar herramientas que son mucho más específicas para bacterias patógenas que los antibióticos actuales, los que tienen como flanco comúnmente vías metabólicas que son muy generales y por lo tanto afectan también a las bacterias beneficiosas de nuestro organismo”, señala la Dra. Bueno.
Una investigación pionera
En una primera etapa de la investigación, que comenzó hace 12 años, el grupo de científicos chilenos del IMII, compuesto por la doctora Bueno y un equipo de estudiantes de pregrado y doctorado, analizaron el cromosoma completo de cepas de la salmonella e identificaron estos segmentos de ADN que se separan del cromosoma. Esta enfermedad causa gastroenteritis aguda, forma parte de la lista de prioridades de la OMS debido a su resistencia antimicrobiana y causa gran mortalidad en países subdesarrollados. A finales del 2018 lograron concluir que la familia de Enterobacterias, a la que pertenece la salmonella, efectivamente es capaz de separar y reintegrar a su cromosoma estos grupo de genes (islas genómicas) que contiene su ADN y los genes necesarios para que la bacteria infecte.
Más tarde, en la segunda etapa del estudio, integrado en su mayoría por mujeres chilenas y publicado en la prestigiosa revista médica PLOS Pathogens, se descubrió que este proceso era fundamental para que la salmonella pudiera generar una infección sistémica. Eso, de hecho, se comprobó en el modelo in vivo en el laboratorio.
“Nosotros les mutamos unas proteínas para que ahora no pudiera sacar estos genes del cromosoma, para que quedaran fijos, y nos dimos cuenta que la bacteria cuando no podía hacer este proceso ya no podía infectar. Ese proceso ocurriría cuando la bacteria está pasando desde el intestino hacia otros órganos”, relata la docente de la Universidad Católica.
¿Una cura del futuro?
Si bien se escogió trabajar con la Salmonella, debido a que diferentes cepas son muy diversas y pueden infectar sólo a humanos, o aves, o ganado, a todos al mismo tiempo; este mismo procedimiento lo comparten otras bacterias patógenas de la familia de Enterobacterias, como lo son el Vibrio cholerae (que produce cólera), la Escherichia coli enteropatógena (que causa el síndrome hemolítico-urémico) y la Klebsiella pneumoniae, una bacteria intrahospitalaria que causa neumonía a los pacientes de riesgo a través de infecciones respiratorias y del tracto urinario.
Bueno explica que con estos datos pueden diseñar fármacos, algún agente antimicrobiano o molécula inhibidora que inactive las proteínas claves de este proceso, evitando que la bacteria siga avanzando, anulando su capacidad de infectar y dejándola susceptible a que el sistema inmune pueda eliminarla fácilmente. Esa es la meta de la siguiente fase de su proyecto. “Eso significaría un tratamiento específicamente para este tipo de Enterobacterias que cada día desarrollan más y más resistencia a los antibióticos que existen”, añade la doctora.
“Ahora a nosotros nos gustaría hacer un estudio un poco más amplio, salirnos del grupo de las Enterobacterias y buscar en otros tipos de bacterias que también son patógenas para ver si tienen elementos parecidos (…) Tenemos la sospecha de que este podría ser un proceso mucho más generalizado en las bacterias que causan enfermedades en el humano”, puntualizó.

En la película de la pandemia, los científicos están trabajando frenéticamente en brebajes para detener la propagación de un virus emergente, y al final, voil, tienen éxito y salvan al mundo. En el mundo real, las vacunas desempeñaron un papel limitado, si es que alguno, en la desaceleración de la epidemia de Zika que azotó a América Latina en 2016, la devastadora epidemia de ébola de África occidental 2014-16 y la pandemia de gripe que comenzó a circular en 2009. Las vacunas simplemente no estaban listas a tiempo.
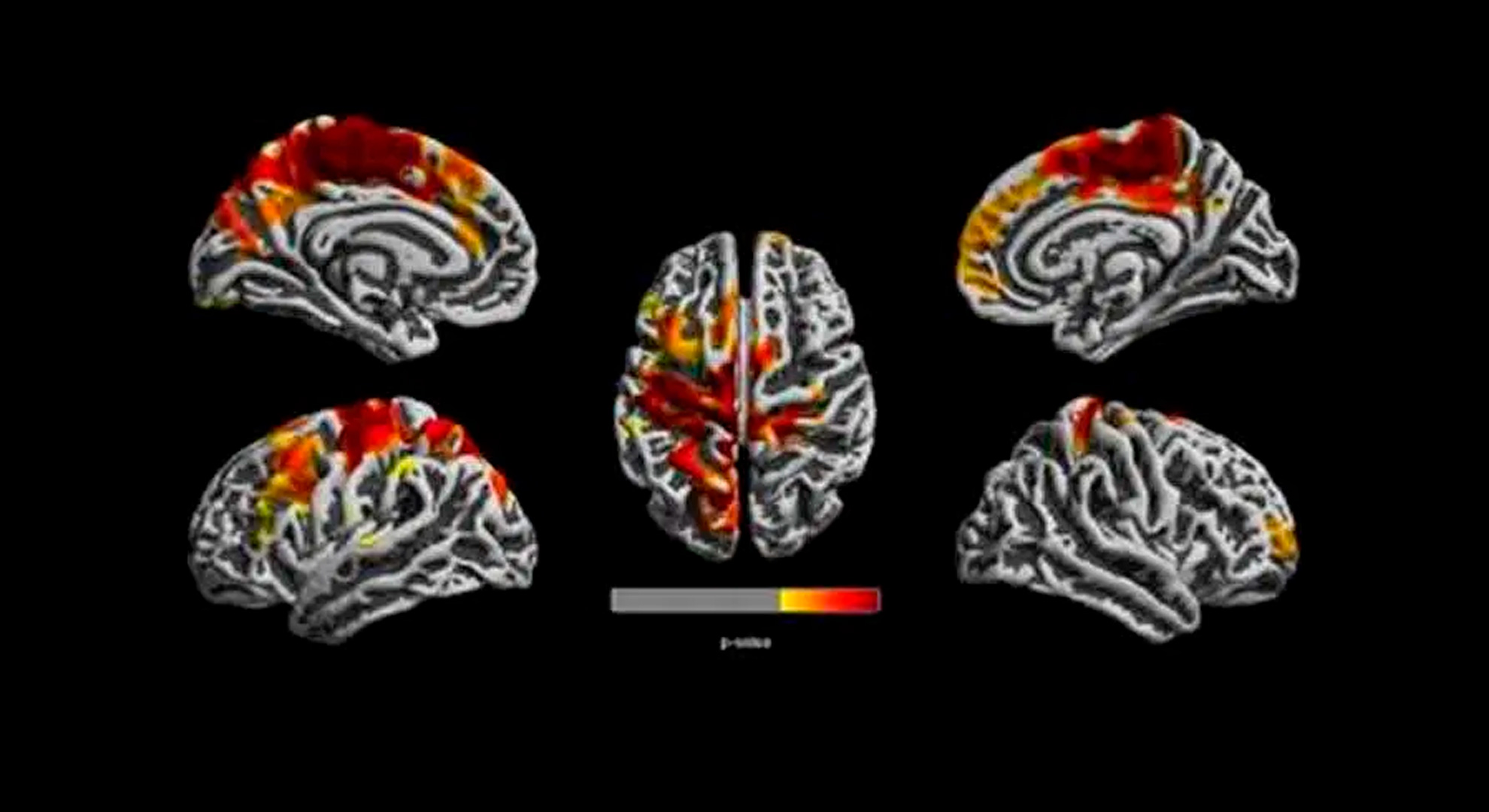
La exposición temprana a altos niveles de contaminación del aire relacionada con el tráfico altera la estructura del cerebro a los 12 años. Los niños expuestos a la contaminación del aire habían reducido el grosor cortical y el volumen de materia gris en comparación con los niños que no estaban expuestos a altos niveles de contaminación.